INSTRUCCIÓN ORTOPÉDICA DE POSGRADO - IMÁGENES
Resolución del caso
Ricardo Trueba
Departamento de Resonancia y Tomografía Computada, Grupo Médico Rostagno, Diagnóstico por Imágenes, Ciudad Autónoma de Buenos Aires, Argentina
Dr. Ricardo Trueba • ricardotrueba@gmail.com
https://orcid.org/0000-0001-7908-817X
https://doi.org/10.15417/issn.1852-7434.2020.85.1.1045
Diagnóstico
Osteoma osteoide en el cuello femoral.
Discusión
El osteoma osteoide es un tumor óseo benigno que tiende a medir menos de 1,5 cm. El tumor puede aparecer en
cualquier hueso del cuerpo, pero es más común en huesos largos, como el fémur y la tibia. Representa entre el 10%
y el 12% de todos los tumores óseos benignos. Puede aparecer a cualquier edad, y es más común en pacientes de
entre 4 y 25 años. Afecta aproximadamente tres veces más a los hombres que a las mujeres.
El osteoma osteoide se caracteriza por un “nidus” asociado a esclerosis ósea reactiva, engrosamiento cortical y
edema óseo. El término “nidus” se refiere al tumor propiamente dicho que está compuesto por hueso en distintas
fases de maduración, en el seno de un estroma constituido por tejido conjuntivo altamente vascularizado. El centro
del nidus, por lo general, es la parte más densamente mineralizada y tiene una cantidad variable de calcificación.
El osteoma osteoide se clasifica, de acuerdo con la localización del nidus, en:
• Cortical (el más frecuente): se asocia típicamente a un engrosamiento cortical fusiforme de la diáfisis de un
hueso largo, con más frecuencia, el fémur y la tibia.
• Intramedular: típicamente localizado en el cuello femoral, en los huesos del carpo y del tarso, y en los elementos
vertebrales posteriores. La esclerosis ósea reactiva suele ser de leve a moderada en esta localización.
• Subperióstico: es más frecuente en el cuello del astrágalo. También suele aparecer en la vertiente medial del
cuello femoral y en los huesos de las manos y de los pies.
Las radiografías revelan típicamente una radiolucidez en el hueso de morfología redonda u ovalada que representa
el nidus (por lo general, <2 cm), el cual muestra una cantidad variable de mineralización central y se acompaña
de un grado variable de esclerosis y engrosamiento cortical adyacente. Puede ser difícil identificar el nidus si
la esclerosis ósea es muy significativa.
La TC proporciona la mejor caracterización tanto del nidus como de la esclerosis ósea que lo rodea. El nidus
se visualiza como una lesión de baja atenuación, bien definida, de morfología redonda u oval y con diferentes
grados de mineralización central. Si hay esclerosis ósea reactiva, esta puede variar de leve a significativa con
reacción perióstica y formación de hueso nuevo, lo cual puede enmascarar el nidus. Estudios de TC con cortes
finos (2-3 mm) en el plano axial, haciendo reconstrucciones multiplanares obtenidas con un algoritmo de hueso y
visualizados con ventana ósea, delimitan mejor el nidus cuando es de pequeño tamaño. Aunque el uso de medio
de contraste intravenoso no es necesario, puede observarse el realce de un nidus hipervascular (no calcificado) en
los estudios de TC dinámicos.
En la RM, el nidus presenta una intensidad de señal baja-intermedia en secuencias potenciadas en T1 y una
intensidad de señal variable en secuencias potenciadas en T2, según la cantidad de mineralización en el centro del
nidus. Debido al aumento de resolución espacial, un nidus calcificado puede ser visualizado como una zona central
de baja intensidad de señal (porción mineralizada) y una periferia de alta intensidad de señal (porción no mineralizada).
Se observa hiperintensidad de señal en la zona reactiva que rodea al nidus en secuencias potenciadas en T2
o STIR cuando hay edema en la médula ósea y en los tejidos blandos adyacentes. El nidus puede mostrar intenso
realce tras la administración de gadolinio intravenoso. Los hallazgos en las imágenes pueden ser inespecíficos y
confundirse con otras patologías (fracturas por estrés u osteomielitis) si el edema circundante es extenso y oculta
el nidus. Con frecuencia, no se pueden detectar nidus de pequeño tamaño en la RM, porque la señal del nidus suele
ser similar a la del hueso cortical.
Diagnóstico diferencial
Los cambios inflamatorios severos pueden dificultar el diagnóstico del osteoma osteoide y simular otros cuadros
diferentes:
• Reacción perióstica prominente y corta edad: osteomielitis o tumor óseo maligno (sarcoma de Ewing).
• Hipertrofia sinovial severa y abundante derrame articular: artritis séptica o artritis crónica inflamatoria.
• Edema significativo de partes blandas y médula ósea que enmascara el nidus: lesión traumática (fractura por estrés) (Figura 7), osteoporosis transitoria (Figura 8) o infección.
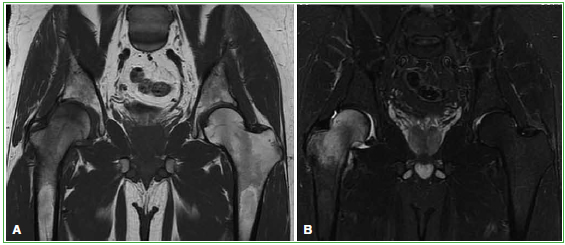
Figura 7. Resonancia magnética de cadera derecha, corte coronal en secuencias potenciadas en T1 (A) y STIR (B). Se
observa edema óseo (aumento de la señal) que afecta a la cabeza y el cuello del fémur, asociado a derrame articular en un
paciente de 30 años.
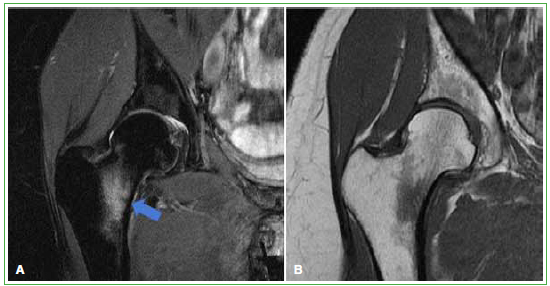
Figura 8. Resonancia magnética de cadera derecha, corte coronal en secuencias potenciadas en STIR (A) y T1 (B).
Se observa edema óseo (aumento de la señal) que afecta al cuello femoral, con un pequeño trazo de fractura trabecular
(flecha) asociado a derrame articular en un paciente maratonista.
El dolor puede aliviarse con medicamentos antinflamatorios no esteroides. El tratamiento varía según la salud
del paciente. Si está sano y el dolor no le provoca una molestia importante, el tumor se trata con agentes antinflamatorios
para aliviar los síntomas. Si esta terapia fracasa o la ubicación del tumor podría causar trastornos del crecimiento,
escoliosis u osteoartritis, se puede considerar la ablación quirúrgica o percutánea. Aunque se demostró
que es eficaz, la resección quirúrgica tiene muchas complicaciones potenciales, como la difícil identificación del
tumor durante la cirugía, la recurrencia local por resección incompleta y la resección del hueso que soporta peso
que puede requerir hospitalizaciones prolongadas y complicar la recuperación (Figura 9).
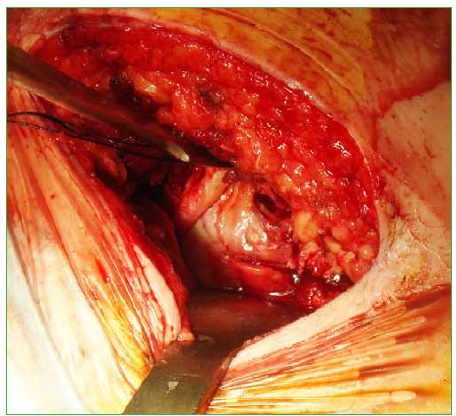
Figura 9. Tratamiento quirúrgico del osteoma osteoide.
Recientemente, la ablación por radiofrecuencia guiada por TC se ha convertido en una alternativa menos invasiva
que la resección quirúrgica. En esta técnica, que se puede realizar bajo sedación consciente, se introduce una
sonda de radiofrecuencia en el nido tumoral, a través de una aguja canulada bajo guía tomográfica y se aplica calor
local para destruir las células tumorales (Figura 10).
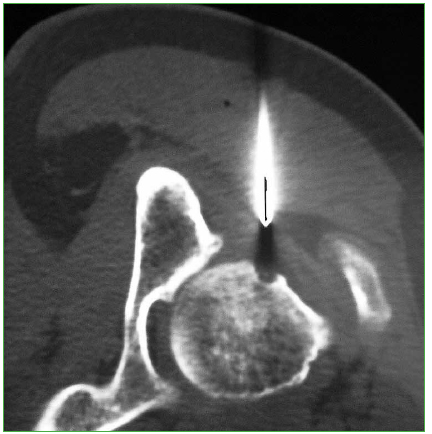
Figura 10. Ablación por radiofrecuencia guiada por tomografía computarizada.
Conflicto de intereses: El autor no declara conflictos de intereses.